冠狀病毒藥物研發與技術情報專輯——冠狀病毒的研究現狀
2019年新型冠狀病毒感染的肺炎疫情爆發後,引 起國際社會高度重視🫲。本文對Cortellis藥物研發綜 合情報平臺的冠狀病毒綜述報告《Disease Briefing: Coronaviruses》(2020年1月30日)重要內容進行摘 編,旨在通過全面梳理冠狀病毒的診斷🎁、預防和治 療的研究進展,為當前疫情的科學研究提供參考🐕。
冠狀病毒是一組有包膜的正義單鏈RNA病毒,屬巢 病毒目(Nidovirales)🤸🏽♂️、冠狀病毒科🧑🏽⚕️、冠狀病毒亞科,已 知26種[5],並根據不同的抗原交叉反應和遺傳組成 被分為4個屬(α、β🎎、γ和δ),其中只有α-和β-屬含有 對人致病的毒株[6]👲。
全球第一例已知冠狀病毒為禽傳染性支氣管炎病 毒,於1937年被分離出來,是引發雞群重度感染的 病原體;第一例人冠狀病毒於1965年由Tyrrell和 Bynoe從人類鼻腔中分離出來,體外擴增結果顯
示,該病毒已在人類中存在至少500-800年,起源於 蝙蝠[7, 8]。
長期以來,冠狀病毒作為重要的動物病原體,可引 發哺乳動物和鳥類的呼吸道及腸道疾病。已知冠狀 病毒中,有6種可引發人類疾病,包括:HCoV-229E🧔🏿♀️、 HCoV-OC43🖤、HCoV-NL63、HCoV-HKU1🦻🏿、SARS-CoV和 MERS-CoV[9, 10]👴🏽。其中,前4種為局部流行性疾病,主 要引起輕度自限性疾病,而後兩種可引發重症[11]。 2002年和2012年發現的SARS-CoV和MERS-CoV屬於 β-冠狀病毒[12],並由於其對人類的高威脅性被列入 WHO高威脅清單[13]。冠狀病毒引發的高患病率對人 類健康構成持續威脅[2]。2019年底在中國武漢爆發 的大規模呼吸系統疾病中分離得到的2019-nCoV, 成為第七個能夠引發人類疾病的離散冠狀病毒種 屬,表征為β-冠狀病毒[14, 15]👱🏿♀️。


圖1 數字彩色透射電子顯微鏡(TEM)圖像 圖片來源:疾控中心/ Fred Murphy; Sylvia Whitfield
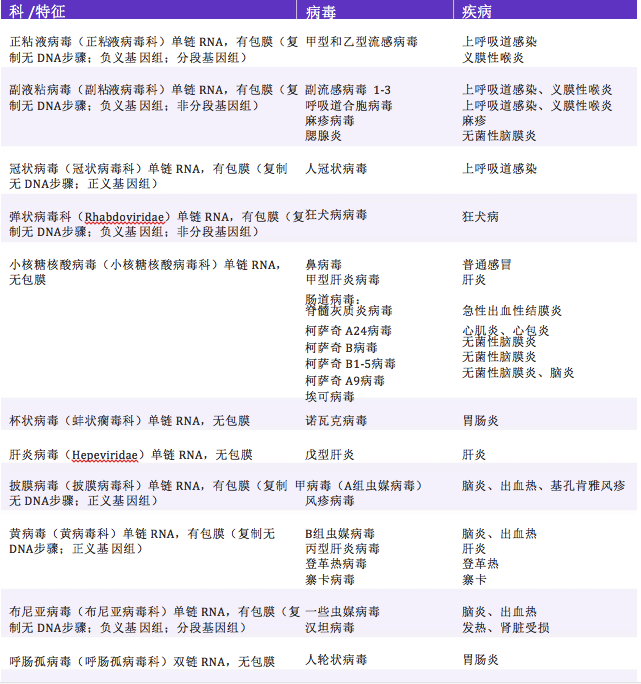
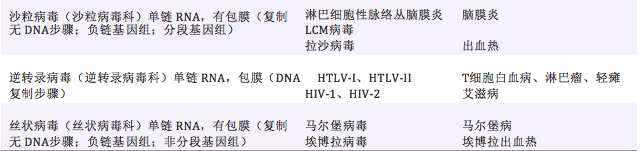
表 1 重要的RNA病毒列表
1. 形態學、結構和復製
“冠狀病毒”因其在電子顯微鏡下呈現的標誌性冠 狀結構而得名,該結構為S糖蛋白在病毒包膜表面 形成的輻射狀刺突[16]。
微觀結構顯示,冠狀病毒包含兩種主要的包膜蛋 白:S糖蛋白和M蛋白。前者是受體結合和細胞融合 的主要抗原[17],後者參與出芽和包膜形成過程,並 在病毒顆粒組裝中發揮關鍵作用[18]。少數冠狀病毒 具 有 第 三 種 糖 蛋 白 ⸺ 血 凝 素 酯 酶 [ H E ] 🫶🏼。此 外 ,病 毒衣殼內的堿性磷蛋白[N]與病毒基因組有密切關 系。冠狀病毒的基因組是非片段正義單鏈RNA,約 26-32kb,是已知最長的RNA病毒基因組,含有7-10個 不同的開放閱讀框(ORF)👩🏻🏫。基因組RNA5’端具有甲 基化帽,3’端具有poly-A尾[17, 19]🧑🏻🌾。
冠狀病毒的高致病性依賴於其靈活的基因重組 和快速的適應性突變。一方面,單鏈RNA在復製 過程中使用的RdRP(RNA依賴性RNA聚合酶)具有 1,000,000個突變/位點/復製的固有錯誤率,可導致 連續點突變;另一方面,當兩種冠狀病毒共同感染 同一宿主時,可從對方的基因組中獲得數百或數千 堿基對的基因組片段,以增加自身生態位點,或成 為新病毒[7, 20, 21],導致了冠狀病毒在約二十年內迅 速變異出三種極具流行潛力的新型人類冠狀病毒: SARS-CoV👩🏿🏭、MERS-CoV和2019-nCoV。
2. 流行病學👨🏼🌾、發病率和死亡率
冠狀病毒可引發人類輕度、自限性上呼吸道感染, 如普通感冒(15%-30%)[16]和肺炎,也可引發人類 胃腸炎以及其它動物疾病[8, 22]😿。
在巴西聖保羅進行的一項為期9年的綜合流行病 學研究顯示,在1137個樣本(包括無症狀個體🗡、普 通患者🚴🏼、並發症患者和重症患者)中,7.7%的呼吸
道樣本檢測到人類冠狀病毒,其中,NL63(50.0%) 和OC43(27.3%)是最常檢測到的冠狀病毒,不同 年份的流行病毒存在差異(如在2004年,HCoV- 229E是流行的主要病毒株(61.5%))[23]。
2014年,對中國北京的559份成人急性呼吸道感染 采樣研究表明,HCoV-OC43的檢出率為12.5%,且在 秋季達到峰值[24]。
同年,對西班牙馬略卡686例急性呼吸道感染成人患 者(2013年1月至2014年2月)的分析顯示,21.6%的患 者與病毒感染有關,其中,7%由冠狀病毒引起,常見 致病菌株為OC43(50.0%)、NL63(29%)和229E(21%)🎧。 研究表明,52%的CoV感染患者需要住院治療,2例患 者需要重症監護,尚無致命的CoV感染[25]。
2016年至2017年,一種新發現的冠狀病毒在中國造 成近2.5萬頭仔豬死亡,該病毒出現在SARS-CoV發源 地附近的馬蹄蝙蝠身上,與2002年的SARS-CoV為同 一種蝙蝠(Rhinolophus spp)。這種新病毒被命名為 豬急性腹瀉綜合征冠狀病毒(SADS-CoV),尚未證實 能感染人類[26]🧜♀️。
2019年底,一種新型冠狀病毒在中國引起發熱性呼 吸道疾病✈️。該病毒暫命名為2019-nCoV,首次在武漢 市中心被檢測到,並被確定來源於武漢市的一家海鮮市場(目前已關閉)。中國的研究機構迅速展開疫 情防控和科學研究,分離出病毒,並進行測序🩱。結果 顯示,2019-nCoV為2B組的β-冠狀病毒,與SARS-CoV的基因序列相似性至少為70%[2]。據WHO統計,截至 2020年1月27日,全球共檢出2798例2019-nCoV確診 病例,其中,中國2741例以及5794例疑似病例,泰國、日本🏍、韓國、美國、澳大利亞和越南等國家報告了孤 立病例和旅行相關病例。截至1月26日,中國確定了 至少80例2019-nCoV感染病例死亡。WHO認為該事件在中國的風險評估為非常高,在區域和全球水平 為高[14, 27]🤷🏽♀️。
3. SARS
SARS(Severe acute respiratory syndrome,即嚴重急 性呼吸綜合征,以下簡稱SARS)是由冠狀病毒引起 的呼吸系統疾病,於2002年11月起源於中國廣東 省,2003年初在亞洲首次報告,隨後在北美和歐洲 報告了類似疾病[28, 29],之後,全球五大洲33個國 家和地區皆有對SARS的報告,其中,中國受影響最大 (香港和北京較嚴重);2003年春,SARS成為全球健 康威脅🧑🏿🎓。研究表明,全球人口的高度流動與疫情的 快速傳播與密切相關[5, 29, 30]。
SARS在全球迅速蔓延引起了高度重視🧔🏻♂️。盡管在 2003-2013年間,SARS再未出現,但專家呼籲,有必 要持續監測該冠狀病毒和相關冠狀病毒,以確保 病毒再次出現時能夠快速應對[31]🏊🏻♂️。各國家/地區高 度重視冠狀病毒引發的疫情:SARS之後,中國政府 在公共衛生🍏、傳染病監測、應對及報告等方面投入 了大量資金,確保國家能夠更有效地應對之後發 生的健康威脅,如H7N9禽流感[32];基於SARS的相 關經驗,國際應對2012年爆發的MERS(中東呼吸綜 合征)時也更加快速👩🔬、有效[12, 33, 34];2019年底,隨著 COVID-19在中國和全球的出現和迅速傳播,相關防 疫經驗再次得到應用[2]。
3.1 SARS病毒
SARS的病原體於2003年3月24日由香港以及美國疾 病控製和預防中心首次報告,並得到細胞培養💆🏽♂️、顯 微鏡檢查、微陣列數據、血清學檢測和PCR等多種 證據支持[35]。2003年4月17日,WHO正式宣布該病原 體為冠狀病毒家族新發現的成員,命名為“Urbani SARS-associated coronavirus”(簡稱SARS-CoV)𓀅。測序 結果表明,SARS-CoV與已知表征過的冠狀病毒僅存 在較遠的相關性[8, 36],此前未在人類身上發現🧑🏿🔬。
在病毒溯源的過程中,未發現健康人群中含有SARS-CoV抗體,表明該病毒未曾在人群中傳播,很 可能起源於動物,突變後導致人類感染。美國和荷 蘭的研究人員通過構建猴感染模型系統,最終證明 了SARS-CoV為病原體[37, 38]🤴。
3.1.1 形態
SARS-CoV病毒顆粒呈球形,平均直徑為 78nm。病毒含有螺旋核衣殼,由包膜包圍[39],其上覆蓋 長約20nm的棒狀長包膜粒,具有典型的冠狀特征🚴🏼。
3.1.2 結構
SARS-CoV的結構與其它冠狀病毒相似, 基因序列為5'端、復製酶[rep]、突刺[S]、包膜[E]🫃🏻、膜 [M]𓀕、核衣殼[N]🧴、3'端,兩端有短的非翻譯區,其他5種 非結構蛋白的序列可能分布於ORF S和N之間。[40]
SARS-CoV的基因組共包含11個ORF,可編碼23個成 熟蛋白[41]👨🏽🏫。其中,兩個主要ORF約占基因組的三分 之二,編碼兩種重要多聚蛋白ORF1a和ORF1b。多聚 蛋白通過蛋白水解裂解產生非結構蛋白,其中最重 要的是RNA依賴性RNA聚合酶(Rep)和ATP酶解旋酶(Hel)💥。不同的SARS-CoV分離株核苷酸序列僅有個 別位點存在差異[42]。
3.1.3 進入
SARS-CoV和普通冠狀病毒類似,通過胞 吞和膜融合進入細胞,受體為ACE2[40, 43]。進入靶細 胞的SARS-CoV可被聚陰離子化合物(該化合物對其 它包膜病毒具有抗病毒活性)抑製,表明SARS-CoV 包膜蛋白可能帶有正電荷,能與靶細胞表面硫酸 乙酰肝素蛋白聚糖上的負電荷發生相互作用[44]。同 時,SARS-CoV需要在酸化的內涵體中才能產生有 效 感 染 ,表 明 其 作 用 存 在 p H 依 賴 性 [ 4 5 ] 。病 毒 R N A 在 一個獨特的瓶狀雙層膜小室中完成復製[46]。研究發 現,SARS-CoV感染在體內和培養細胞都可引起超微 結構改變,包括形成雙膜囊泡🏯、細胞質中出現核衣 殼包涵體和顆粒[39]。
3.1.4 復製
研究顯示,病毒RNA聚合酶起始轉錄完 整負鏈,生成mRNA,其亞基因組轉錄是嵌套的,具 有相同的5’端非翻譯區和3’端的poly-A尾。病毒 RNA聚合酶與重復基因間序列(TRS,轉錄調節序 列)相互作用,允許5’前導序列與每個基因的起始 序列之間連接🥈。目前,病毒的復製機製尚不明確,研 究人員推測可能通過含有反前導序列的亞基因組 大小的負鏈RNA進行。其他證據顯示,在被SARS-CoV 感染的細胞中可觀察到含有病毒RNA和蛋白的大 顆粒區域,而在其它冠狀病毒感染的細胞中未觀察 到,由此推測,這些區域可能是SARS病毒的翻譯中 心[39]🌰。
3.1.5 組裝
病毒顆粒在高爾基體中裝配,在擴張的 囊泡中累積,然後被轉運並分泌到細胞表面,通過 胞吐作用釋放。
3.1.6 生物學特性
SARS-CoV的生物學特性不同於已 知冠狀病毒,主要表現在以下2方面:
1)S蛋白中存在一個短錨點:小ORF的數量和位置不 同;只有一個PLP-蛋白酶;核衣殼蛋白中存在一個 獨特的短賴氨酸富集區😯。這些變異的生物學意義尚 不清楚[42, 47]。
2)對Vero細胞(一種來源於非洲綠猴腎上皮細胞的 細胞系)有嗜熱性;與其它在低溫下生長的冠狀病 毒不同,可在37°C下生長,並可感染下呼吸道[44]。
3)SARS-CoV基因組大小在29705―29751個核苷酸 之間[48]🥗。SARS病毒基因組與之前已知的三組冠狀 病毒均不匹配,與冠狀病毒229E和OC43僅有較弱 的抗原關系𓀏。聚合酶基因與第2組的牛和鼠冠狀病 毒密切相關,但也具有第3組禽冠狀病毒的一些特 征。SARS-CoV不具有存在於第2組和某些第3組冠狀 病毒中的血凝素-酯酶,但具有存在於第3組冠狀病 毒中的單一木瓜蛋白水解酶[49]。鑒於此,SARS-CoV 單獨劃分為第4組[42, 47],與三個已知組在系統發育 上等距🧖♂️。其他研究發現了兩種該類病毒:HCoV-NL63 (2004)和HCoV-HKU1(2005),二者均遍布全球,而前者至少已在人群中傳播數百年[8, 50, 51]。
3.1.7 起源
早期研究表明,SARS-CoV與牛、鼠肝炎冠 狀病毒有關,但測序結果未發現有牛-鼠來源,因此 研究人員推斷,SARS-CoV是一種新的未知病原體, 而不起源於已有病毒株[41]。相關研究推測,該病毒 可能來源於冠狀病毒的祖先,在越過人類物種屏障 導致SARS之前已自然感染野生動物[7],並由動物與 人類病毒之間重組而產生[7]。通過貝葉斯系統發育 幹擾等方法,已證明SARS-CoV基因組在RNA聚合酶 基因內具有重組斷點:5'區域與哺乳動物冠狀病毒 相關,3'區域與禽冠狀病毒相關[52]🪢。
2003年5月,香港科學家報道稱在一種罕見的果子 狸(Civettictis civetta)(一種樹棲貓)中發現了一種 病毒,與引起SARS的病毒幾乎相同。香港大學的袁 國勇指出,這種冠狀病毒是從生活在巴基斯坦-印 度尼西亞一帶的一種棕櫚果子狸的糞便中發現的。 2002年11月,最早出現的SARS病例中就有動物食品 加工售賣經營者和廣東省參與準備野味宴會的廚 師🤾🏿♂️。香港大學的研究小組能夠從所有25只果子狸中 培養出與SARS-CoV幾乎相同的冠狀病毒,代表了8 種不同的被檢測物種[53]。
另一個研究小組在廣東省出售食用活體動物中檢 測到了SARS-CoV樣病毒💪🏿。同時,有研究發現喜馬拉 雅棕櫚果子狸(Paguma幼蟲)(Paguma larvata)和浣 熊犬(Nytereutes procyonoides)中也均有該病毒[7]👾。測序結果顯示動物和人病毒之間存在系統發育差 異,隨後的研究表明,SARS-CoV在果子狸中的傳播 時間並不長,其它物種可能作為天然宿主,如蝙蝠 [28,54-55]✉️🏈。
之後,相關人員對疫區進行了血清學分析,結果顯 示,約40%野生動物經銷商和20%屠宰從業人員攜 帶有SARS-CoV抗體。研究人員推測,在SARS爆發前 至少兩年,該地區已存在SARS樣冠狀病毒,且該類 病毒起初在人群中並不具備感染性,可能經過進化 適應後,變成SARS-CoV [8]。
3.2 傳播
SARS-CoV可通過飛沫和直接接觸傳播[56]。病毒在痰 液中的濃度可達到約1億粒/ml[57],在室溫條件下可 在受汙染表面和物體上存活長達6天[5]。
導致SARS迅速蔓延的主要因素包括:(1)航空旅行 導致的全球人口高度流動;(2)高密度的城市人口 導致的人類頻繁接觸[58]🌠。
在疫情爆發期間,醫療機構的發病率高於50%,而 庭傳播比例較低(6%-8%)[59, 60]。之後的模擬研究 表明,醫生和其他醫護人員是醫院環境中SARS傳播 的主要媒介[5]:一方面,呼吸和霧化支氣管擴張劑等的使用可能導致氣溶膠的形成和含有病毒的飛沫擴散;另一方面,心肺復蘇、支氣管鏡檢查、氣管 插管術1️⃣👩🦼➡️、吸痰也可能增加病毒傳播的風險[5, 61, 62]。而外科口罩🧝🏽♂️、手套和防護服的使用則可有效減少院內 傳播[63]👩👩👦。
臨床研究顯示,病毒載量和傳播高峰出現在有臨床 症狀的第10天左右,此時病情惡化⸺因此,患者 在尋求醫學救治時感染性最強[5, 64]🕵🏼。其他研究表明, 病毒的傳播可持續13天以上(範圍2-60天)[5];此外, 潛伏期患者無感染性[65]♢。
在 病 毒 傳 播 過 程 中 ,“ 超 級 傳 播 者 ” 受 到 高 度 關 註 [ 5 , 6 6 ] 。研 究 表 明 ,超 級 傳 播 似 乎 與 高 病 毒 滴 度 、氣 溶 膠😙、環境汙染以及在醫療環境中與其他人的密切接 觸有關[5]。
在醫學檢測方面,冠狀病毒的RNA可以在血清轉化 後長期存在,且連續數周可在呼吸道分泌物👩🏻🦽➡️、血漿 和糞便中檢測到[5],因此,采取措施降低醫院感染 風險具有重要意義[67]🤳。
3.3 症狀和疾病
呼吸道是SARS-CoV的主要侵襲部位。SARS-CoV最常 感染下呼吸道,引發嚴重的急性病毒性肺炎🕵️♂️。WHO 對疑似SARS的病例定義包括高熱(>38°C)或在過去 48小時內有發熱史;胸部X射線檢查顯示肺炎的新 浸潤;流感樣症狀(寒戰、咳嗽、不適、肌痛)或SARS- CoV暴露史;以及SARS的一項或多項陽性診斷檢測 [5]。但SARS最初的症狀和臨床表現很難與其它常見 的呼吸道感染區分開來,老年人可能沒有發熱。
對屍檢樣本和實驗感染動物的分析表明,SARS-CoV 感染會影響肺部區域,並可在2型肺細胞中被檢測 到[21]。研究指出,SARS-CoV在組織中常引起彌漫性 肺泡損傷、支氣管上皮剝脫、纖毛缺失和鱗狀上皮 化生,一些病例中也觀察到巨細胞浸潤👨👩👦、噬血細胞 增多症和腫大的肺泡上皮細胞[68]。感染經過炎症 期或滲出期(特征為透明膜形成⏪🛳、肺細胞增生和水 腫)、增生期和纖維化期[21]。
除了呼吸道感染外,胃腸道[69]、中樞神經系統也出現了感染病例[69, 70]。臨床特征顯示,SARS症狀的出現通常遵循三階段模式:(1)感染後的第1周,症狀通常包括發熱和肌痛。這些早期症狀可能與直接的病毒細胞病變效應有關,可通過PCR檢測到病毒載量的增加;(2)第2周檢測到血清轉化,隨後病毒 [71]; 載量降低 (3)20%的感染患者臨床特征為病情惡 化,病毒復製失控。該階段可能是過度免疫應答觸 發免疫病理損傷的結果,而過度免疫應答可能是 SARS引起肺損傷的最終原因[21]。
在SARS疫情爆發期間,患者的臨床表現不完全相 同。約100%的成人和兒童出現發熱,約一半出現咳 嗽和/或肌痛,只有少數患者有上呼吸道症狀;11%- 15%的就診患者和高達40%-70%的住院患者報告了 腹瀉[5, 30];部分患者出現淋巴細胞減少症、白細胞減 少症、血小板減少症;其他患者出現乳酸脫氫酶🎋、天 門冬氨酸氨基轉移酶和肌酸激酶等酶水平升高,表 明SARS對某些患者的肝臟產生影響[5, 57]。此外,也有 患者出現急性腹痛等其他症狀[72];胸部X射線可檢查到肺浸潤,主要是細胞因子和趨化因子導致[21]; 40%的感染患者發生呼吸衰竭,需要輔助換氣,而90%的患者在首次出現症狀後一周內恢復。對特定 人群的研究發現:吸煙者比不吸煙者更需要機械換氣[72];老年患者發病率和死亡率較高[73, 74],幼兒群體的感染率和感染強度較低[8],10歲以下兒童發病率 僅為1%[76]。
在致死率方面,24歲以下患者的死亡率<1%[54],60歲 以下患者中上升至約13%,60歲以上患者和發生急 性呼吸窘迫綜合征的患者死亡率高達約50%[5, 74]🥨。 據統計,疫情爆發期間的總死亡率約為10%,致死 病例的特征為幹擾素刺激異常🫲、持續性趨化因子應 答,以及適應性免疫應答失調[74]🥂☠️。
其他不良臨床結果的獨立相關因素包括已知的糖 尿病/高血糖症病史[75]、高齡、男性⚁、並發肝炎👩🏻🎤、入院時中性粒細胞計數高及高水平的乳酸脫氫酶,以及 空氣汙染和宿主遺傳變異[5,54,74]。
在患者預後方面,2007年報道的一項前瞻性研究首 次提供了關於SARS幸存者長期愈後的全面信息🤠。來 自安大略省多倫多市的117名SARS幸存者在出院後 的三個不同時間段(3、6和12個月)接受了體檢🙍🏿、肺功 能檢測、胸部X射線檢查和6min步行試驗👫🏻。結果表明, 大多數SARS幸存者在一年前已從疾病中完全恢復。 但SARS幸存者在患病一年後的總體健康📑、生命力和 社會功能均低於正常水平,許多患者反映無法恢復 到SARS前的工作水平🀄️。在評估期間,心理健康醫療資 源的使用率顯著高於正常水平[77]。隨後對多倫多22 名長期幸存者的研究確定,在發病後會出現持續長 達20個月的症狀,包括肌肉骨骼疼痛、疲乏、抑郁和 睡眠障礙[78]👨🏽✈️。香港研究人員的一項長期隨訪還發現, 在隨訪的第四年,233名SARS幸存者有顯著的精神疾 病和持續性疲乏[79];另外一項香港隨訪研究表明,醫務工作者多遭受長期損害[80]。
3.4 流行病學與經濟損失
在2002年11月1日至2003年8月7日期間,WHO報告了 全球33個國家共8,422例SARS病例和916例死亡病例 [81]🛍️。其中,中國受影響最嚴重,感人人數超過5,327人(占總感染人數的66%),死亡人數達349人(占總死 亡人數的45%)[32]🙆🏿👰🏻♀️。流行病學研究估算SARS的平均潛 伏期為6.4天,年輕患者的死亡率為6.8%,60歲以上患 者的死亡率為43%[5],全球病死率為11%[56],各地區之 間存在顯著差異[82]🤞🏼🧑🏽💼。
除了國民健康,SARS流行對經濟也產生了重要影響🔈。據估計,全球SARS流行的經濟損失約為300億美元, 東亞的年經濟增長率下降1個百分點[83],中國的總經濟影響為253億美元[32],僅北京旅遊部門的損失達14 億美元[84]。
盡管SARS對人類健康和經濟造成了重大影響,但回 首整個疫情的防控過程,研究人員👨💼、醫療機構和醫 療主管部門之間達成了前所未有的國際合作,並有 效遏製了SARS在全球的快速蔓延 [8, 66, 82]。
4. MERS
MERS(Middle East respiratory syndrome,即中東呼吸 綜合征,以下簡稱MERS)是由新型β冠狀病毒MERS- CoV引發的急性呼吸道疾病。2012年9月,WHO報告 了兩例由已知的人冠狀病毒引起的急性呼吸道疾 病病例,患者出現腎功能衰竭並最終死亡[16, 85]。目 前已知的最早病例可追溯至2012年4月[7]。之後研究 表明,引發該疾病的病毒可能來源於蝙蝠[12],單峰 駝為其中間宿主[86];MERS-CoV與SARS-CoV存在遺傳 學差異[87],且與後者不同,其細胞受體為二肽基肽 酶4(DPP4亦名CD26)[88, 89]。在人肺上皮細胞試驗中, MERS-CoV可引起不同模式的宿主基因表達反應🤵🏻♀️。由 於該病毒可引起人畜共患疾病並且病死率較高(約 35%),因此在全世界引起廣泛關註[89]。WHO已發布 對疑似感染者進行適當護理的中期指南[90, 91]📑🕎。
4.1 MERS病毒
MERS病毒(以下簡稱MERS-CoV)是一種有包膜的正義單鏈RNA病毒,基因組大小為29.9 kb🪚。該病毒是已 發現的第一種可感染人類的β冠狀病毒屬成員,與蝙蝠冠狀病毒(例如HKU4和HKU5)的親緣關系比與SARS-CoV更接近 。血清流行病學研究未能發現 [16, 92] MERS-CoV在受疫情影響地區的普通人群中引起既 往感染的證據,從而確認這是一種新型病毒[16]。
MERS-CoV的基因組排列為5'-復製酶-結構蛋白(刺 突-包膜-膜-核衣殼)-pol(y A)-3',與其它冠狀病毒相 似🖖🏻🙆🏽♀️。該病毒有10個ORF和16個假定的非結構蛋白參 與病毒轉錄和復製過程[10, 16]。
MERS-CoV通過與腎臟和其它器官中表達的DPP4受 體結合而進入宿主細胞[51],利用宿主蛋白酶進入肺 細胞🧏🏻♀️🧏🏿♀️。furin可激活病毒包膜上的S蛋白,介導膜融合 和病毒進入宿主細胞[92]。與SARS-CoV一樣,MERS- CoV能夠攻克宿主的天然免疫應答,產生高病毒滴 度,誘導細胞因子失調[10, 21]⚔️。
4.2 傳播
研究猜測MERS-CoV起源於蝙蝠,但其從蝙蝠傳播到 人類宿主的機理最初尚不清楚[51]⛹🏼♀️。研究者首先確定 了其中間宿主為單峰駝[9, 92, 93],同時推測了幾種可 能的傳播途徑:直接接觸(特別是幼年駱駝),體液、 處理肉類及/或食用未經巴氏消毒的駱駝奶[12, 94]💇♂️。 MERS-CoV起初被證實是人畜共患病毒,隨後研究 發現,53%-60%的病例存在人與人之間的非持續傳 播,並主要聚集在衛生保健機構內和家庭成員之間👩🏽🎓,後續研究表明,飛沫和環境接觸都可導致病毒傳播[86, 94, 95]。
4.3 症狀和疾病
MERS-CoV感染的潛伏期約為5天(範圍在2-15天), 94%的患者在第12天時出現疾病體征[16]。
MERS-CoV感染的典型的症狀非特異性,臨床表現包 括輕度/無症狀感染🤵🏻♀️👳♀️、重度感染性肺炎、急性呼吸窘 迫🏘、膿毒性休克和導致死亡的多器官功能衰竭等[11, 12]🥅。同時,部分患者伴有ARDS和多器官功能障礙綜合 征的呼吸衰竭,且多數出現並發症的患者需要在症 狀出現後2-5天內入住重症監護病房👯。這些患者從症 狀發作發展到需要采取有創通氣和/或體外膜肺氧 合的中位時間為4.5-7天[16,34]。統計顯示,嚴重疾病風 險較高的人群主要包括年齡在45歲以上並存在糖尿 病👼🏼、肥胖症🤞🏽、慢性腎臟疾病、慢性心臟病和COPD等既 往病史的男性以及醫護人員[11, 16]🔌。
MERS爆發早期,病死率接近60%;隨著疾病防範意 識和檢測技術的提升,死亡率有所下降,但仍維持 在35%以上[96, 97]。與年輕患者相比,50歲以上患者的 死亡率更高(分別為77%和22%)[98],且男性患者和 有基礎疾病的患者死亡率較高[16, 92]。
4.4 流行病學
自2012年9月以來,累計27個國家報告了MERS-CoV 的感染病例,包括意大利👩🏽🎓、荷蘭、法國、德國🤹🏻、意大 利♻、突尼斯👳🏽、馬來西亞👨🏿🦱、英國、美國、伊朗、埃及、黎 巴嫩和土耳其等[97, 99]。初始病例限於中東地區和在 英國確診的2例感染,後者為之前去沙特阿拉伯旅 行被感染患者的家庭成員。之後出現了群聚性感染(包括沙特阿拉伯的一次醫院感染),從而證實病 毒在密切接觸期間可在人與人之間傳播[12, 100]。截 至2019年11月,各國已向WHO通報2494例經實驗室檢測確認的人感染病例和780例相關死亡(病死率 37.1%)[14]。然而,統計學研究指出,已發表的流行病 學數據僅反映有MERS臨床表現的患者數量,但無 症狀疾病的發生率更高。根據對2012年12月至2013 年12月期間被醫療專業人員接診和參與疾病研 究個體的血清調查,估算沙特阿拉伯約45000人為 MERS-CoV血清學檢測陽性[101]💅🏿。此外,對2012年9月 至2016年前往受MERS影響國家的旅行者進行的一 項研究推測這些國家(沙特阿拉伯、阿拉伯聯合酋 長國、約旦和卡塔爾)嚴重感染者達3300人,約為確 診總數的2.3倍[102]📦。
2015年5月20日,韓國報告了首例確診病例,出現了 沙特阿拉伯王國以外國家/地區最大規模的MERS- CoV疫情爆發。該首例確診患者曾前往中東四個國 家,返回韓國時仍無症狀。截至9月11日,已向WHO 通告了韓國的185例實驗室確診病例和36例死亡病 例,以及中國的一例病例[99]。
MERS感染的流行病學呈現出一定的季節性發病特 點,2013年🙌🏽、2014年和2015年春季的爆發時間與駱 駝分娩月份一致[96]。
MERS-CoV的基本再生數(R0)小於0.7―表明產生大 流行的可能性較低[12]。但相關研究人員仍建議,加強 疾病監測和對接觸者的主動追蹤,並徹底調查可能的動物宿主和人畜共患疾病再感染的途徑,避免疫 情持續[12, 103]。
5. COVID-19
2019年底,武漢爆發了新型冠狀病毒感染的肺炎 (COVID-19)[104,105]📀。測序顯示,該疾病的病原體2019- nCoV為sarbecovirus亞屬β冠狀病毒,與SARS-CoV的 基因序列相似性為75%-80%[2-4]。據推測,蝙蝠可能 是其動物宿主,同時可能存在中間宿主[4]。WHO的風 險評估認為疫情在中國的情況為極高風險,在區域 和全球的情況為高風險[14, 27,106]。
6. 診斷
2002年SARS爆發初期,SARS的診斷主要基於臨床 特征和陽性病例流行病學史[5]。臨床特征顯示,與 SARS相關的症狀包括高熱(>100.4°F/38°C)、咳嗽和 呼吸困難。如果有與肺炎或呼吸窘迫綜合征相符的 浸潤性病竈,可通過胸部X射線檢查確診。臨床數據 顯示,部分患者在出現症狀2周內可檢測到抗SARS 病毒抗體,發熱3周後可獲得明確診斷👏🏿。
在SARS流行期間,FDA和CDC聯合進行了SARS診斷 檢測的驗證和許可👱🏻♂️。診斷性檢查的方法主要包括 血清學檢測、細胞培養分離病毒、電子顯微鏡檢查 和PCR檢測。此外,Suresh,MR等人還研發了針對冠 狀病毒抗體的ELISA檢測法和免疫熒光血清學檢測 法等,可用於SARS檢測[107]🧎🏻♀️➡️📉。各類檢測方法各具特色: (1)ELISA法的可靠性和特異性高,但需在症狀出 現後約20天才可檢出,無法滿足快速診斷的需求 [107]; (2)免疫熒光檢測法可在症狀出現10天後在血清中檢測到抗體,但需進一步排查🧏🏻♀️。如症狀出現4周 後血清檢測為陰性,則排除SARS [108];(3)細胞培養 物中和電子顯微鏡檢查在常規性診斷中存在靈敏 度不高🚣🏼♂️、操作不便捷的局限性;(4)RT-PCR是唯一能 夠用於早期臨床檢測的快速診斷方法,檢出率為 37.5%-50%[107]◼️。SARS爆發期間,多用兩步常規和一 步定量RT-PCR進行檢測[110],而實時RT-PCR可在病毒 滴度較低的疾病早期階段進行檢測[111]𓀋。
研究表明,SARS患者可檢測出的病毒RNA量隨感染 時間的推移不斷增加,並在第10天左右達到峰值。 臨床數據顯示,感染後第一周的初始階段,可在患 者的鼻咽抽吸物🫱🏼、咽拭子和痰液樣本中檢測到病 毒,而感染後期更容易在糞便樣本中檢測到病毒[109];部分患者在發病一個月後仍可從呼吸道分泌物 中檢測出SARS-nCoV,但病毒較難分離培養🤟🏻🥯。
MERS爆發期間,除上述SARS的檢測方法外,還使用了蛋白質微陣列🍼、微量血清中和試驗以及蛋白質印跡等方法。結果顯示,RT-PCR檢測仍是所有方法中特異性和敏感性最高的方法[10,92]。2013年6月,美國FDA批準了CDC新型冠狀病毒2012實時RT-PCR檢測試劑盒的緊急使用許可,允許有資質的實驗室將其用於檢測呼吸道✤、血液和糞便樣本檢測🍃。同期, WHO建議靶向upE基因篩查,並針對陽性樣本進行ORF1a、ORF1b或N基因復檢,同時建議使用從病毒載量最大的下呼吸道獲得樣本檢測[92]。為減小創傷性取樣的應用,有時也會用從上呼吸道采集的樣本代替[16]。此外,德克薩斯大學和美國國立衛生研究院研發了針對MERS檢測的不對稱5引物逆轉錄環介導的等溫擴增(RT-LAMP)技術,用於擴增位於ORF1a和ORF1b基因以及upE基因內的MERS-CoV基因組位點,並擬進一步開發便攜式即時檢驗診斷試
除以上特異性檢測方法外,冠狀病毒的診斷方法還 包括鑒別診斷:(1)由肺炎鏈球菌、流感嗜血桿菌、 卡他莫拉菌🕵🏼♀️、耐甲氧西林金黃色葡萄球菌和軍團菌 等引起的肺炎,必須納入SARS的鑒別診斷;(2)季節 性流感和禽流感⏬🦶🏼、呼吸道合胞病毒感染、水痘帶狀 皰疹病毒感染🛑、人偏肺病毒感染以及漢坦病感染等 發熱性病毒感染也建議納入鑒別診斷👩🏿🚀。此外,在適 當的情況下,還需考慮將其它流行性或影響人群較 廣的疾病(如天花👲🏿、土拉熱病、炭疽、病毒性出血熱 或鼠疫等)也納入鑒別診斷[5]👩🏽⚕️。
7. 預防
由於冠狀病毒感染患者通常存在潛伏期(SARS 2-14天(平均4天)[5],MERS 2-15天(平均5天)[92]),且在潛伏期內往往無特異性症狀,因此對於冠狀病毒的感染預防工作往往需要政、醫和科研界等多方配合🏣🆎。在尚無有效的抗感染藥物或疫苗階段,隔離、檢疫和消毒等幹預措施是控製具有大流行潛力的冠狀 病毒感染的最有效手段[16, 113]。
政府應綜合考慮防控帶來的經濟和社會影響,及時 采取防控措施。相關研究表明,政府采取積極的防 控措施對疫情控製有明顯成效:新加坡實施有效的 SARS感染控製措施,將R0從第1周的7降至第2周的 <1[5];臺灣實施A級檢疫(疑似SARS患者的潛在暴露 接觸者)減少了約461例新增病例和62例死亡病例; 相比之下,使用B級檢疫(來自受疫區的旅行者)僅 使新增病例和新增死亡人數減少約5%[34, 114]。
在醫護人員的防控方面,建議醫護人員使用包括護 目鏡在內的個人防護設備,以及外科口罩或一次性 N-95過濾呼吸器[16];同時,采取空氣傳播預防措施, 尤其在進行諸如插管等可能產生氣溶膠的操作過程 [115];此外,應謹慎處理和運輸所有疑似感染性標本, 必須在符合WHO BSL3標準的實驗室進行檢測[16]。
此外,用肥皂🎼、酒精洗手對阻斷病毒傳播有一定效 果。相關數據顯示:(1)SARS病毒能夠在表面存活長 達6天,但使用漂白劑🙅🏿♂️、75%乙醇♋️、家用清潔劑[5]、化學 消毒劑(如聚維酮碘)或加熱都可將其滅活[56];(2) MERS病毒在20°C下可存活長達48小時,在30°C下可 存活24小時[16]🗑。
除上述措施外,作為人類預防病毒感染的重要方 法,疫苗具有重要意義。但疫苗的研發過程涉及病 毒株的分離🛟、動物實驗和臨床試驗等嚴格流程,需 要較長時間,截止目前,尚無已獲批上市的針對冠 狀病毒感染的有效疫苗🟣。
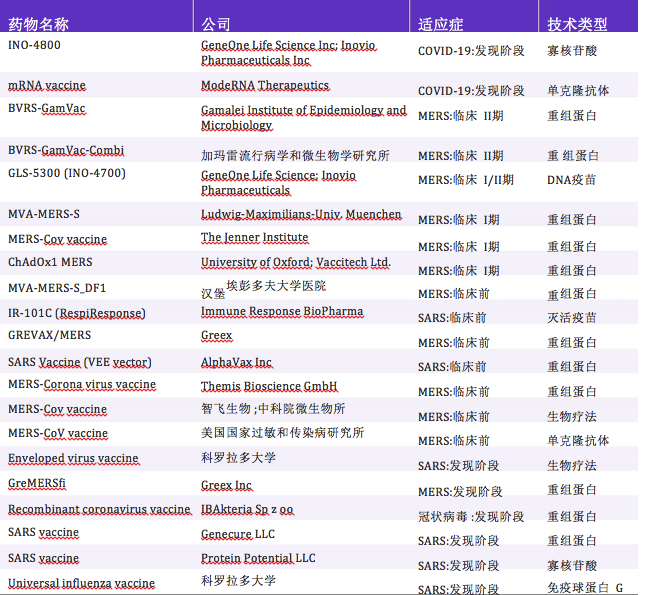
迄今為止,針對冠狀病毒感染的在研疫苗共21種, 2種處於COVID-19的早期發現階段(見表2)🏚。研究顯 示,S蛋白目前被認為是冠狀病毒疫苗開發最有希望的靶點之一,並正被用於抗人冠狀病毒疫苗的研發(如用於鼻內給藥的黏膜疫苗,人類MERS-CoV疫苗(包括DNA疫苗🛍️、基於載體的減毒活疫苗和蛋白質亞單位疫 苗)[86,89,117-120]。
此外,研究發現腺病毒相關疫苗可誘導SARS-CoV特異 性T細胞和病毒中和抗體應答[121]。有研究指出,這兩 種反應對持久性免疫保護非常重要:在對已治愈SARS 患者的長期研究中,抗體應答在大約6年後減弱,而T 細胞應答持續存在,表明後者是建立長期免疫所必需的[12]📙。在中東地區爆發MERS期間,相關人員還優先研 發了用於駱駝的疫苗,以阻斷該疾病在人畜之間的傳播[11,116]🫸🏼。
總體而言,近年來在冠狀病毒引發的疫情期間,國際社會高度響應,多方配合密切,從前期的疫情防控過程中不斷積累經驗。WHO還專門針對SRAS疫情和MERS疫情的爆發修訂了其成員國報告傳染病的規則,有效提高了國際社會應對疫情爆發的反應速度和協作力度 [16,122]🥷🏼。
表 2 冠狀病毒在研疫苗詳情
8. 治療
2003年SARS爆發期間,早期治療方法主要為經驗性[30]:治療 (1)早期研究表明,來自人免疫血清球蛋白的廣譜抗體治療方法對SARS效果不明顯,其他非特 異性免疫抑製劑或廣譜抗病毒藥物(如利巴韋林)[125,126]; 的治療效果也相對有限 (2)臨床試驗顯示,利巴韋林和皮質類固醇聯合療法被在一線治療中取 得了一定效果🧙🏽🎻。但該結果未在體外實驗中獲得證實[5, 127]; (3)為減輕副作用,部分治療方案將皮質類固醇給藥延遲到感染的第二周;(4)HIV蛋白酶抑製劑 洛匹那韋/利托那韋作為單藥治療或與利巴韋林聯合使用可阻斷SARS-CoV病毒的復製;(5)HIV蛋白酶 抑製劑奈非那韋被建議作為備選藥物[30]。
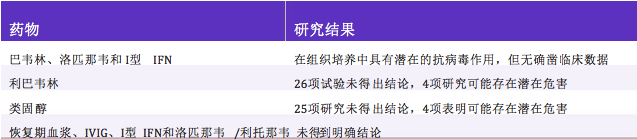
WHO對2002-2003年SARS爆發期間使用的所有已發 表藥物治療報告進行了總結(包括6類藥物和72項 研究),結果顯示,沒有任何確鑿證據表明針對SARS 患者有特效治療藥物(見表3)。相關人員指出,臨床 試驗的設計應考慮標準化方案(劑量和治療時間 標),並持續監測臨床數據[128]。同時,當疫情再次出 現,應在負壓單人病房中隔離SARS感染的確診患 者,並應使用合適的口罩盡量降低病毒通過呼吸道 分泌物傳播的可能性[5]。
在MERS爆發後,美國國立衛生研究院篩選了290種 已批準並具有明確細胞靶點的試驗藥物,用以驗證 其對SARS和/或MERS的療效。結果顯示,33種化合 物對MERS-CoV有活性,6種對SARS-CoV有活性,27種 對兩種冠狀病毒均有活性。活性藥物分為13個治療 類別,包括抗菌藥和抗寄生蟲藥、神經遞質抑製劑、 雌激素受體拮抗劑👨🏿💻、激酶信號抑製劑🛀、脂質或固醇 代謝抑製劑🥯、蛋白加工抑製劑和DNA合成/修復抑 製劑[129]。在另一項研究中,荷蘭研究者在一個由348 種FDA批準的藥物組成的化合物庫中篩選具有抗 MERS-CoV活性的藥物,發現其中4種(氯喹、氯丙嗪、 洛哌丁胺和洛匹那韋)可在低微摩爾濃度下抑製 MERS-CoV復製,並建議在動物模型中進一步進行藥 物評價👊🏼。研究顯示,MERS-CoV感染患者使用這些藥物的過程中,即使不能100%有效阻斷病毒復製,也 可以為患者的免疫系統爭取對感染產生應答的窗 口期[130]🏊♀️。此外,有研究指出,洛匹那韋/利托那韋和 幹擾素-β-1b聯合使用在普通狨猴中產生了極好的 治療效果,有進一步研究的價值[124]。
表 3 SARS感染藥物治療研究結果
8.1 皮質類固醇
皮質類固醇在SARS爆發期間被廣泛使用。在一家中 國臨床試驗中心接受治療的225例SARS患者中,使 用皮質類固醇使OI從平均237mmHg的基線值增加 到類固醇給藥後的335mmHg,最佳劑量為1-3mg/kg(或160-240mg /d),總累積劑量為1000-2000mg,最 佳療程為8-14天[131]。香港一家醫院在治療過程中發現,疾病早期階段給藥會延長病毒血症持續時間, 因此僅在SARS感染後期脈沖給藥甲基潑尼松龍作 為搶救療法[54]。
盡管糖皮質激素治療對OI有積極影響[131],但回顧性 研究表明,該治療方法的結局並不理想[128]🐅。基於上 述經驗,MERS患者在使用皮質類固醇進行治療時 相對謹慎[2]。同時,建議在COVID-19患者的常規治療 中盡量避免使用該類藥物[1]。
8.2 廣譜抗病毒藥物
利巴韋林是一種核苷類似物,對某些冠狀病毒以及 呼吸道合胞病毒和偏肺病毒具有活性👸。作為廣譜抗 病毒藥物,利巴韋林是首批用於抗SARS臨床療效檢 測的化合物之一🔞。早期研究表明,利巴韋林(或與皮 質類固醇聯用)治療SARS的效果差異較大[5]。其他 動物研究實驗表明,在恒河猴的MERS-CoV感染模型 中,利巴韋林和IFN-a2b聯用可減少病毒復製、調節 宿主反應📏、改善臨床效果[132]。然而,對2012年10月至 2014年5月在沙特阿拉伯接受聯合治療的20例患者 進行的一項回顧性研究顯示,盡管與標準治療相比 利巴韋林/IFNα-2a聯合治療明顯提高了患者的14天 生存率,但28天後的生存率無顯著差異[133]。此外,利 巴韋林會帶來大量副作用,包括劑量依賴性貧血、 心律不齊、胸痛和頭暈等不良反應[5]⛸。
除利巴韋林外,目前沒有其他廣譜抗病毒藥物,這 與病毒缺少共同藥物靶點有關。有研究表明,鈣調 磷酸酶/NF-AT通路在CoV感染宿主的免疫細胞活化 中發揮重要作用,而環孢菌素的無免疫抑製活性的 衍生物有可能幹擾這一過程,從而作為廣譜冠狀病 毒抑製劑發揮作用[134]。
8.3 病毒酶抑製劑
病毒酶抑製劑主要作用於冠狀病毒復製的特定步驟,如:(1)進入抑製劑或膜融合抑製劑可阻斷病毒 與宿主細胞的融合;(2)病毒蛋白酶抑製劑可阻斷 聚合酶蛋白的裂解以抑製病毒RNA合成;(3)核苷類 抑製劑可特異性抑製病毒復製而不損傷宿主細胞; (4)絲氨酸蛋白酶靶向抑製劑可阻斷病毒生命周期的後期過程。(5)許多宿主蛋白酶可對決定 [19, 136]; [19, 135] 病毒進入的S蛋白進行水解加工,包括組織蛋白酶、弗林蛋白酶和胰蛋白酶 (6)II型跨膜絲氨酸蛋白酶(TMPRSS2)等其他激活S蛋白的酶,也可視為 潛在靶點[19, 89]🍵。;
藥物試驗結果顯示,蛋白酶抑製劑和洛匹那韋/利托那韋聯用在抗MERS-CoV方面取得了較大進展。其中,幹擾素-β1b和洛匹那韋/利托那韋聯合治療的臨床前評價取得成功(狨猴模型中的死亡率顯著降低),並有待進一步的臨床評價[16]。此外,正在進行的MIRACLE試驗旨在評估洛匹那韋/利托那韋聯合重組幹擾素-β1b對MERS-CoV感染患者的有效性和 安全性[137]💁。
基於以上經驗,武漢的醫院對早期收治的COVID-19 患者進行了洛匹那韋和利托那韋聯合治療,同時迅 速啟動了隨機對照試驗,以評價聯合用藥治療這種 新型冠狀病毒感染的有效性和安全性[1]🖖🏽。
此外,解旋、裝配和胞吐等環節也被視為潛在的治 療靶點,但目前僅在體外和動物模型中有效,尚未在人體中實驗[11,138]。
8.4 幹擾素
幹擾素在SARS的體外試驗和臨床治療中顯示出一 定效果。
德國法蘭克福大學醫學院的研究人員評價了β-幹擾 素、α-幹擾素和γ-幹擾素對來自法蘭克福和香港患 者SARS-CoV菌株的抗病毒活性,並在Vero和Caco-2 細胞系中進行了復製[139]👱🏿。結果顯示,β-幹擾素表現出良好的抗病毒活性,在兩種細胞系中均可抑製SARS-CoV的復製;α-幹擾素也具有一定活性,但敏感性指數是β-幹擾素的/90―1/50;γ-幹擾素在其中一 種細胞系的活性略高於α-幹擾素,但在另一種細胞系中完全無活性[140]。體外研究中,MERS-CoV對α-幹 [51] 擾素治療的敏感性是SARS-CoV的50-100倍 。
加拿大研究人員研究了在多倫多一家醫院聯合使 用幹擾素α-1和皮質類固醇治療SARS疑似患者的 效果🉑。該醫院共9例患者接受了聯合治療,13例患者 接受了皮質類固醇治療🤣。結果顯示:兩種治療方法 對發熱和白細胞減少的效果相似,但聯合治療(分 別為33.3%和11.1%)組比單藥治療組(分別為38.5% 和23.1%)轉入重症監護病房和需要插管的發生率 低,且聯合治療組無死亡,單藥治療組的死亡率為 7.7%🥇。此外,聯合治療組患者的胸部X射線檢查在4 天內轉為正常,而單藥治療組為9天[141]。
2003年6月初,Amarillo Bioscience宣布在中國大陸 和臺灣地區分發低劑量口服幹擾素α錠劑,用於 SARS的潛在治療和預防🅿️。前期動物實驗表明,每日 一次口服小劑量幹擾素α,持續四天,可顯著降低感 染傳染性胃腸炎冠狀病毒(TGEV)的仔豬的死亡率▶️。
此外,有研究表明,在19種被批準用於臨床的抗病 毒藥物中,Alferon N(幹擾素α-n3)對SARS-CoV具有 較強的抗病毒活性[142]。
8.5 免疫調節劑
SARS期間,中國政府批準使用免疫系統增強劑進 行治療,如賽生公司的日達仙(胸腺肽α1,在中國上 市,用於治療乙型肝炎的免疫系統增強劑),雖未得 到有效數據支持,但仍被看作治療SARS和其它感 染性疾病的潛在治療藥物[143]🫠。有研究猜測,利巴韋 林可減少被感染小鼠體內促炎性細胞因子的釋放, 作為免疫調節劑發揮作用[144],但體外研究表明,能 夠抑製其它病毒的利巴韋林濃度不足以抑製SARS- CoV的復製[145]🧛。因此,一些治療成效可能歸因於其 免疫調節活性[146]。
此外,在SARS流行期間,還使用了其他免疫調節的 治療方案,如靜脈註射免疫球蛋白和恢復期血漿[127, 147]👴🏻。
MERS期間,部分韓國患者接受了恢復期血漿治療。 一些醫療數據庫和“灰色文獻”描述了使用恢復期 血漿🤜🏼☝️、血清或來源於恢復期血漿的高免疫球蛋白治 療病毒引起的嚴重急性呼吸道感染,但回顧性分析 表明該方法安全,並有可能降低死亡率[147]🤏。沙特阿 拉伯科學家報道稱,由於合適供體的數量有限,評 價該療法的臨床試驗將面臨許多困難[148]👩❤️💋👨。
8.6 單克隆抗體
單克隆抗體(MAbs)通常是防禦新發疾病的一線技術🪞。其中,免疫原性較低的全人源化抗體是首選種類[149]。
Dana-Farber癌症研究所分離出一種80R抗體,可阻 斷病毒與ACE2受體結合,動物模型檢測表明該抗體 可預防急性肺損傷,預期可以被動免疫的方式用於 SARS-CoV感染的早期治療[5, 150]👨🏿🎓。隨後的研究表明,該 抗體對另一種不同的SARS-CoV毒株無效[5]。
美國國家癌症研究所研究了兩種新的抗體m396和S230.15,二者對ACE2受體的親和力均>80R。建模 研究顯示,兩種抗體可中和SARS-CoV的毒株,推測其可能適用於未來SARS感染的診斷、預防和/或治療[151]。
美國和中國研究人員的一項合作研究從候選抗體 中鑒定出三種MERS-CoV靶向受體結合域(CD26/ DPP4)的單克隆抗體,並進行了體外評價🪦。結果顯 示,MAb m336中和病毒的效價很高,有巨大潛力為候選治療藥物[152]。此外,日本研究人員還研究了 針對MERS-CoV CD26的單克隆抗體,並確定了人源 化MAb YS110作為候選藥物的潛力,且進行了用於 其它適應症的臨床試驗[153]👨🦱。
8.7 藥物研發管線
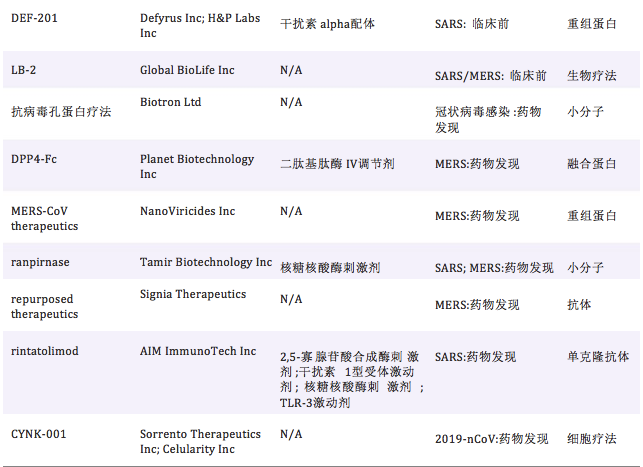
當前,針對冠狀病毒的藥物研發管線共23個,主要 涉及以上6種藥物類型,詳見表4🐻❄️。
表 4 當前抗冠狀病毒藥物研發管線
8.8 治療靶點
當前,對冠狀病毒的藥物靶點研究持續進行,已驗證的靶點主要集中於病毒脫殼、釋放、復製、翻譯、 組裝、形成衣殼、出芽等步驟(見圖2、圖3)。

圖 2 SARS-CoV感染靶點全景
註:箭頭表示正效應;橫線表示負效應🫁🦖。灰色或淺色符號是未經驗證的蛋白質靶點(即,未處於活性開發階段[UAD])。紅色邊框內的粉 紅色文本框表示已驗證的基因靶點。黃色文本框代表未驗證的基因靶點。紫色和粉紅色文本框分別表示細胞外和細胞內效應。綠色文 本框表示相關疾病/病況/症狀。

圖 3 MERS-CoV感染靶點全景
註:箭頭表示正效應;橫線表示負效應。灰色或淺色符號是未經驗證的蛋白質靶點(即,未處於活性開發階段)。紅色邊框內的粉紅色文 本框表示已驗證的基因靶點☂️。黃色文本框代表未驗證的基因靶點。紫色和粉紅色文本框分別表示細胞外和細胞內效應。綠色文本框表 示相關疾病/病況/症狀。






